je vous informe que j'ai quitté mon poste de vice présidente de l'apnée du sommeil et je continuerai a vous informer sur la maladie indépendamment de l'association .
donc je vous rermercie de me lire et surtout prenez soin de vous
https://www.facebook.com/midjach
mercredi 28 mars 2012
dimanche 18 mars 2012
L’apnée du sommeil, une maladie méconnue
Ce trouble prive le dormeur d’un sommeil réparateur

Francis A-Trudel @
Le Journal de Montréal, Publié le: | Mise à jour:
photo d’archives
Ce trouble prive le dormeur d’un sommeil réparateur
Ronfler comme un ours peut camoufler l’apnée du sommeil, un problème aux conséquences beaucoup plus sérieuses que le simple mal de côtes, résultat d’un excès de coups de coude de la part de votre partenaire de lit…
Maladie méconnue des Québécois, l’apnée du sommeil affecte un adulte sur six.C’est pourquoi l’Association pulmonaire du Québec et Dave Morissette, atteint de ce trouble respiratoire depuis 10 ans, s’associent pour lancer une campagne de sensibilisation à la maladie et à ses symptômes.
« L’apnée du sommeil est une condition encore peu connue du public. De ce fait, elle est plus difficile à identifier, d’autant plus que ses principales manifestations ont cours pendant que la personne dort. Un patient peut donc vivre des symptômes très désagréables pendant longtemps avant de se savoir atteint », explique la directrice de l’Association pulmonaire du Québec, Dominique Massie.
Effets sournois
Il s’agit d’une maladie aussi sournoise que les conséquences qu’elle entraîne. « On parle de changements d'humeur pouvant aller jusqu’à la dépression, de somnolence durant la journée, de perte de libido et même d’hypertension », énumère Mme Massie.
Alors qu’il plonge vers les profondeurs du sommeil, le dormeur atteint d’apnée doit remonter à la surface jusqu’à une centaine de fois par nuit pour prendre une bouffée d’air, alerté par un signal d’asphyxie lorsque ses voies respiratoires se ferment complètement entre deux ronflements. Chaque remontée, en l’occurrence un imperceptible réveil, interrompt sa descente vers un repos réparateur.
L’ancien dur à cuire du Canadien de Montréal, Dave Morissette, témoigne. Avant d’être diagnostiqué, il se réveillait au matin comme s’il n’avait pas dormi de la nuit. « Au cours de la journée, je devais lutter contre la fatigue et je peinais à me concentrer plus que 15 minutes », raconte-t-il.
Changer une vie
Si l’ex-hockeyeur a eu la chance d’être diagnostiqué, il encourage les gens à se rendre sur ronflercommeunours.com afin de passer le test. L’Association pulmonaire a mis ce site en ligne pour démystifier la maladie et aider les gens à la reconnaître.
M. Morissette rappelle qu’il s’agit « d’un problème sérieux, mais facilement identifiable et, surtout, traitable, pour lequel il existe une solution ».
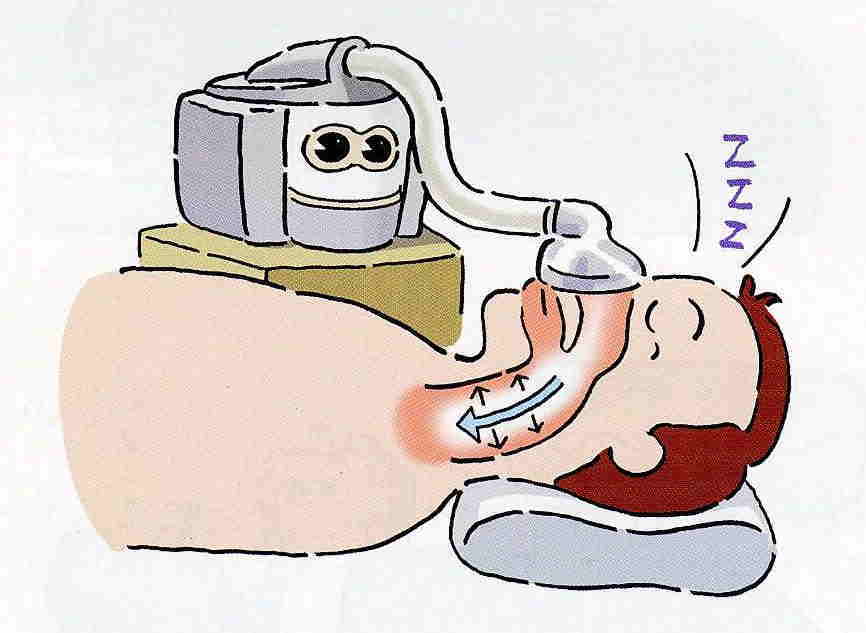
La sienne ? Dormir avec un masque raccordé à une machine qui envoie un jet d’air régulier au fond de sa gorge de façon à maintenir les voies respiratoires ouvertes.
L’effet « Darth Vader » passé, comme il le décrit lui-même, et un temps d’adaptation qui peut aller jusqu’à quatre semaines, la personne sentira une nette amélioration.
La Journée mondiale de l’apnée du sommeil sera soulignée le 18 mars 2012
Maladie méconnue des Québécois, l’apnée du sommeil affecte un adulte sur six.C’est pourquoi l’Association pulmonaire du Québec et Dave Morissette, atteint de ce trouble respiratoire depuis 10 ans, s’associent pour lancer une campagne de sensibilisation à la maladie et à ses symptômes.
« L’apnée du sommeil est une condition encore peu connue du public. De ce fait, elle est plus difficile à identifier, d’autant plus que ses principales manifestations ont cours pendant que la personne dort. Un patient peut donc vivre des symptômes très désagréables pendant longtemps avant de se savoir atteint », explique la directrice de l’Association pulmonaire du Québec, Dominique Massie.
Effets sournois
Il s’agit d’une maladie aussi sournoise que les conséquences qu’elle entraîne. « On parle de changements d'humeur pouvant aller jusqu’à la dépression, de somnolence durant la journée, de perte de libido et même d’hypertension », énumère Mme Massie.
Alors qu’il plonge vers les profondeurs du sommeil, le dormeur atteint d’apnée doit remonter à la surface jusqu’à une centaine de fois par nuit pour prendre une bouffée d’air, alerté par un signal d’asphyxie lorsque ses voies respiratoires se ferment complètement entre deux ronflements. Chaque remontée, en l’occurrence un imperceptible réveil, interrompt sa descente vers un repos réparateur.
L’ancien dur à cuire du Canadien de Montréal, Dave Morissette, témoigne. Avant d’être diagnostiqué, il se réveillait au matin comme s’il n’avait pas dormi de la nuit. « Au cours de la journée, je devais lutter contre la fatigue et je peinais à me concentrer plus que 15 minutes », raconte-t-il.
Changer une vie
Si l’ex-hockeyeur a eu la chance d’être diagnostiqué, il encourage les gens à se rendre sur ronflercommeunours.com afin de passer le test. L’Association pulmonaire a mis ce site en ligne pour démystifier la maladie et aider les gens à la reconnaître.
M. Morissette rappelle qu’il s’agit « d’un problème sérieux, mais facilement identifiable et, surtout, traitable, pour lequel il existe une solution ».
La sienne ? Dormir avec un masque raccordé à une machine qui envoie un jet d’air régulier au fond de sa gorge de façon à maintenir les voies respiratoires ouvertes.
L’effet « Darth Vader » passé, comme il le décrit lui-même, et un temps d’adaptation qui peut aller jusqu’à quatre semaines, la personne sentira une nette amélioration.
La Journée mondiale de l’apnée du sommeil sera soulignée le 18 mars 2012
mardi 6 mars 2012
information complète sur l'apnée du sommeil et ses dérivés
Bonjour ,
Je vous suggère de lire le site internet sur l'apnée du sommeil , très bien fait et surtout très complet .
http://neurobranches.chez-alice.fr/sommeil/sas.html
Bonne lecture
Je vous suggère de lire le site internet sur l'apnée du sommeil , très bien fait et surtout très complet .
http://neurobranches.chez-alice.fr/sommeil/sas.html
Bonne lecture
Merci a SOS clinique du sommeil
Merci a la clinique SOS de la France ,qui m' apermis de reproduire les recherches sur l'apnée du sommeil .
Bonne lecture
Bonne lecture
LE SYNDROME D'APNÉES OBSTRUCTIVES DU SOMMEIL (SAOS)
'individualisation du syndrome d'apnées obstructives du sommeil (SAOS) est
relativement récente puisqu'elle remonte en 1976. Il reste que l'existence de
troubles respiratoires nocturnes est connue depuis l'Antiquité et que Charles
Dickens nous a laissé une
description remarquable du tableau clinique, que le corps médical
dénommera bien plus tard le " syndrome de Pickwick ". Les études
épidémiologiques indiquent clairement qu'il s'agit d'une pathologie fréquente
touchant 2 à 4% de la population adulte. Dans les centres d'études du sommeil,
ce syndrome d'apnées est à l'origine de 43 à 59% des consultations pour
hypersomnolence diurne et de 6 à 29% des consultations pour insomnie chronique.
Encore insuffisamment reconnu, le SAOS se caractérise par la survenue répétitive
d'apnées obstructives et d'hypopnées au cours du sommeil. La survenue de ces
événements respiratoires nocturnes induit une importante désorganisation de la macrostructure comme de la
micro architecture du sommeil. De part le retentissement sur la
vigilance diurne de ces troubles du sommeil, le SAOS a un net impact sur la
qualité de vie des patients. Tant les conséquences socioprofessionnelles des
troubles de la vigilance que les fréquentes complications cardio- et
cérébro-vasculaires du SAOS en font un véritable problème de santé
publique.
Le SAOS se définit par la survenue répétitive, au cours du sommeil, d'obstructions complètes ou partielles des voies aériennes supérieures, responsables d'apnées ou d'hypopnées.
En fait, une valeur d'IAH n'a de sens que si elle est associée à des signes cliniques. La sévérité d'un SAOS ne peut se réduire à un index mais doit tenir compte de l'invalidité que représente l'hypersomnolence, de la souffrance physique et relationnelle des patients, des répercussions du syndrome sur le système cardio-respiratoire et sur le système nerveux.
Le SAOS est caractérisé par la répétition d'occlusions complètes (apnées) ou incomplètes (hypopnées) du pharynx. Cette région anatomique est complexe et est constituée de parois comportant des muqueuses, des muscles et des aponévroses. On remarque que le pharynx n'est constitué d'aucune structure rigide pour les soutenir et offre donc une grande susceptibilité à la déformation. Une anomalie des voies aériennes ou des muscles respiratoires peut n'entraîner aucun trouble pendant le jour grâce à des systèmes compensateurs, dont la perte pendant le sommeil peut favoriser l'apparition d'apnées.
DEFINITION
Le SAOS se définit par la survenue répétitive, au cours du sommeil, d'obstructions complètes ou partielles des voies aériennes supérieures, responsables d'apnées ou d'hypopnées.
- Une apnée est définie par l'arrêt du flux aérien durant plus de 10 secondes, cet arrêt pouvant être d'origine centrale (absence de commande respiratoire), obstructive (obstruction des voies aériennes supérieures avec persistance des efforts ventilatoires) ou mixte (c'est à dire d'origine centrale puis obstructive). Au cours des apnées obstructives, la contraction des muscles respiratoires est incapable de faire entrer l'air dans les poumons du fait de l'obstruction des voies aériennes supérieures. Les apnées peuvent s'accompagner de micro éveils.
- Il n'existe aucun consensus sur la définition des hypopnées. La recherche de la survenue d'hypopnées suppose une mesure quantitative, et non plus seulement qualitative, de la ventilation. A ce jour, la définition la plus utilisée est une diminution de la ventilation (du flux aérien) d'au moins 50 % pendant au moins 10 secondes, diminution associée à une désaturation artérielle en oxygène d'au moins 4%. Les hypopnées peuvent aussi s'accompagner de micro éveils.
- On calcule alors un index d'apnées-hypopnées, soit le nombre d'apnées et d'hypopnées par heure de sommeil :
IAH = (Nombre d'apnées + Nombre d'hypopnées) / Durée du Sommeil (mn) x 60
En fait, une valeur d'IAH n'a de sens que si elle est associée à des signes cliniques. La sévérité d'un SAOS ne peut se réduire à un index mais doit tenir compte de l'invalidité que représente l'hypersomnolence, de la souffrance physique et relationnelle des patients, des répercussions du syndrome sur le système cardio-respiratoire et sur le système nerveux.
PHYSIOPATHOLOGIE DU SAOS
Le SAOS est caractérisé par la répétition d'occlusions complètes (apnées) ou incomplètes (hypopnées) du pharynx. Cette région anatomique est complexe et est constituée de parois comportant des muqueuses, des muscles et des aponévroses. On remarque que le pharynx n'est constitué d'aucune structure rigide pour les soutenir et offre donc une grande susceptibilité à la déformation. Une anomalie des voies aériennes ou des muscles respiratoires peut n'entraîner aucun trouble pendant le jour grâce à des systèmes compensateurs, dont la perte pendant le sommeil peut favoriser l'apparition d'apnées.
CALIBRE ET FORME DES VOIES AÉRIENNES SUPÉRIEURES
A l'éveil, la forme des voies aériennes supérieures (VAS) est différente entre
les sujets non ronfleurs, ronfleurs non apnéiques et apnéiques. L'augmentation
de l'épaisseur des parois pharyngées latérales, des dépôts graisseux le long des
parois pharyngées induisent une compression latérale des VAS.
Toutes les anomalies morphologiques des VAS, comme une micrognathie, une rétrognathie, une hypertrophie de la base de la langue, favorisent et sont fréquemment associées à un SAOS. Il existe, en outre, une inflammation de la muqueuse des VAS chez les sujets apnéiques. Cette inflammation joue sur la collapsibilité des VAS par le biais d'une diminution de leur calibre lorsque le tonus vasculaire augmente. Des signes de souffrance musculaire à type de fibrose et d'dème ont également été décrits dans certains muscles des VAS.
Ces anomalies sont de plus en plus marquées en fonction de l'importance des troubles respiratoires au cours du sommeil. De fait, elles témoignent des conséquences du traumatisme des VAS lié à la vibration tissulaire nocturne. Ces modifications tissulaires jouent elles-mêmes un rôle dans les propriétés mécaniques des tissus des VAS.
L'élastance de la luette, reflet de la rigidité tissulaire, est plus élevée chez les patients apnéiques que chez les ronfleurs et ce, par dème, inflammation et fibrose des tissus péri musculaires associés à une plus grande proportion de tissu adipeux. Ainsi, l'index d'apnée augmente proportionnellement à l'élastance de la luette et, malgré une plus grande capacité à générer une tension des muscles dilatateurs des VAS chez le sujet apnéique (cf. infra), le déplacement tissulaire est moindre du fait d'une inefficacité de transmission de cette force dilatatrice aux tissus mous.
Toutes les anomalies morphologiques des VAS, comme une micrognathie, une rétrognathie, une hypertrophie de la base de la langue, favorisent et sont fréquemment associées à un SAOS. Il existe, en outre, une inflammation de la muqueuse des VAS chez les sujets apnéiques. Cette inflammation joue sur la collapsibilité des VAS par le biais d'une diminution de leur calibre lorsque le tonus vasculaire augmente. Des signes de souffrance musculaire à type de fibrose et d'dème ont également été décrits dans certains muscles des VAS.
Ces anomalies sont de plus en plus marquées en fonction de l'importance des troubles respiratoires au cours du sommeil. De fait, elles témoignent des conséquences du traumatisme des VAS lié à la vibration tissulaire nocturne. Ces modifications tissulaires jouent elles-mêmes un rôle dans les propriétés mécaniques des tissus des VAS.
L'élastance de la luette, reflet de la rigidité tissulaire, est plus élevée chez les patients apnéiques que chez les ronfleurs et ce, par dème, inflammation et fibrose des tissus péri musculaires associés à une plus grande proportion de tissu adipeux. Ainsi, l'index d'apnée augmente proportionnellement à l'élastance de la luette et, malgré une plus grande capacité à générer une tension des muscles dilatateurs des VAS chez le sujet apnéique (cf. infra), le déplacement tissulaire est moindre du fait d'une inefficacité de transmission de cette force dilatatrice aux tissus mous.
LES MUSCLES DILATATEURS DES VOIES AÉRIENNES SUPÉRIEURES
La contraction des muscles inspiratoires (essentiellement du
diaphragme) crée une dépression négative, c'est à dire inférieure à la pression
atmosphérique, ce qui attire l'air dans les poumons. Cette pression négative a
tendance à fermer le conduit des VAS.
Normalement, un mécanisme protecteur est mis en jeu avant même le début de l'inspiration par la contraction des muscles dilatateurs du pharynx. L'activité électromyographique phasique des muscles dilatateurs précède celle des muscles respiratoires.
En outre, l'activité tonique des muscles oropharyngés est un élément important du maintien de la perméabilité des VAS, une diminution de cette activité tonique s'accompagnant d'une diminution de volume des VAS. En fait, toute modification de l'activité des muscles dilatateurs du pharynx va modifier la collapsibilité des VAS. Ainsi, les activités toniques et phasiques des muscles des VAS diminuent avec le sommeil, de façon variable d'un muscle à l'autre.
Outre le sommeil, les muscles dilatateurs sont sensibles aux stimuli métaboliques (hypoxie, hypercapnie) et mécaniques (pression négative dans les VAS). Il faut noter à ce propos les effets délétères de l'alcool et de certains médicaments comme les benzodiazépines qui dépriment l'activité des muscles pharyngés.
Mais, il apparaît, en fait, que l'activité du muscle génioglosse est plus élevée chez les patients apnéiques que chez les sujets normaux à l'endormissement, au cours du sommeil mais surtout à l'éveil.
Les caractéristiques histochimiques et métaboliques des fibres musculaires des muscles pharyngés et laryngés varient entre les sujets apnéiques et ronfleurs simples, l'ensemble des muscles pharyngés et laryngés des sujets ronfleurs et apnéiques semblant faire face à une adaptation physiologique en réponse à un exercice de type résistif répété supra maximal prolongé : hypertrophie musculaire - augmentation de la proportion des fibres IIA à contraction rapide – augmentation des activités enzymatiques de la voie anaérobique ... On ne peut donc pas invoquer une simple diminution de l'activité des muscles dilatateurs oropharyngés dans le sommeil pour expliquer l'obstruction des VAS dans le SAOS.
Normalement, un mécanisme protecteur est mis en jeu avant même le début de l'inspiration par la contraction des muscles dilatateurs du pharynx. L'activité électromyographique phasique des muscles dilatateurs précède celle des muscles respiratoires.
En outre, l'activité tonique des muscles oropharyngés est un élément important du maintien de la perméabilité des VAS, une diminution de cette activité tonique s'accompagnant d'une diminution de volume des VAS. En fait, toute modification de l'activité des muscles dilatateurs du pharynx va modifier la collapsibilité des VAS. Ainsi, les activités toniques et phasiques des muscles des VAS diminuent avec le sommeil, de façon variable d'un muscle à l'autre.
Outre le sommeil, les muscles dilatateurs sont sensibles aux stimuli métaboliques (hypoxie, hypercapnie) et mécaniques (pression négative dans les VAS). Il faut noter à ce propos les effets délétères de l'alcool et de certains médicaments comme les benzodiazépines qui dépriment l'activité des muscles pharyngés.
Mais, il apparaît, en fait, que l'activité du muscle génioglosse est plus élevée chez les patients apnéiques que chez les sujets normaux à l'endormissement, au cours du sommeil mais surtout à l'éveil.
Les caractéristiques histochimiques et métaboliques des fibres musculaires des muscles pharyngés et laryngés varient entre les sujets apnéiques et ronfleurs simples, l'ensemble des muscles pharyngés et laryngés des sujets ronfleurs et apnéiques semblant faire face à une adaptation physiologique en réponse à un exercice de type résistif répété supra maximal prolongé : hypertrophie musculaire - augmentation de la proportion des fibres IIA à contraction rapide – augmentation des activités enzymatiques de la voie anaérobique ... On ne peut donc pas invoquer une simple diminution de l'activité des muscles dilatateurs oropharyngés dans le sommeil pour expliquer l'obstruction des VAS dans le SAOS.
IRRÉGULARITÉS RESPIRATOIRES DANS LE SOMMEIL ET DÉCLENCHEMENT DES APNÉES
Plusieurs arguments supportent actuellement l'hypothèse que les irrégularités respiratoires, telles que l'alternance d'hypo et d'hyperventilations, sont en fait à l'origine des apnées obstructives :
- Celles-ci sont presque exclusivement observées dans le sommeil lent léger et au cours du sommeil paradoxal, où il existe des fluctuations physiologiques de la ventilation mais pratiquement jamais au cours du sommeil lent profond, où la respiration est très stable et régulière.
- La respiration au cours du sommeil reste périodique après trachéotomie chez les patients porteurs d'un SAOS
- L'induction de phénomènes de respiration périodique dans le sommeil s'accompagne d'obstructions des VAS chez l'homme normal ...
Il existe, de fait, au cours des périodes d'hypoventilation, une baisse de l'activité des muscles oropharyngés comme un retard d'activation de ces muscles par rapport aux muscles respiratoires – retard de contraction des muscles dilatateurs observé dans la majorité des apnées obstructives. L'origine d'une telle instabilité respiratoire chez le patient apnéique reste à élucider, l'augmentation des résistances des VAS pouvant elle-même induire une instabilité respiratoire.
EPIDEMIOLOGIE DU SYNDROME D'APNÉES DU SOMMEIL
FACTEURS JOUANT SUR LA PRÉVALENCE DU SAOS | |
 |
La prévalence du SAOS augmente
nettement avec l'âge et ce, surtout après 60 ans. Dès les premières études, il est apparue une nette prédominance masculine. Le rôle des hormones sexuelles est confirmée par l'augmentation de la prévalence des troubles respiratoires nocturnes chez la femme après la ménopause. L'administration d'hormones mâles provoque l'aggravation d'un SAOS chez l'homme et l'apparition d'un SAOS chez la femme. La grande fréquence des obèses parmi les patients atteints de SAOS est une notion classique. Le rôle de l'obésité, essentiellement l'obésité tronculaire (ou androïde), est confirmé par la diminution de l'IAH après une perte de poids. Il existe également une association nette entre SAOS et ronflements. |

|
Une relation entre la
prévalence des apnées nocturnes observées par l'entourage et la consommation
d'alcool a
été retrouvée chez les hommes dans une enquête de terrain récente. La plupart
des auteurs penchent pour un effet direct de l'alcool sur les muscles
dilatateurs du pharynx. En concordance avec une association tabagisme ronflements, on retrouve une proportion significativement plus élevée de SAOS chez les fumeurs. Après ajustement sur l'âge, le poids, la consommation de café et d'alcool, le risque relatif est 3 fois plus élevé chez les fumeurs. Il existe une prévalence très élevée des anomalies ORL chez les patients atteints de SAOS - surtout l'obstruction nasale. |
 |
Certaines études arguent en
faveur de l'existence d'un facteur génétique, trouvant une prévalence exceptionnellement élevée (47%) de
troubles respiratoires nocturnes chez les fils de 45 patients présentant un
SAOS. Des familles présentant plusieurs patients atteints d'un SAS ont été
décrites dans la littérature. Cette ségrégation familiale s'explique par le fait
que la plupart des facteurs de risques impliqués dans la physiopathologie des
SAS sont largement déterminés génétiquement (obésité, alcoolisme, facteurs
anatomiques osseux et des tissus mous qui prédisposent à l'obstruction des voies
aériennes supérieures). Des différences de configuration anatomique des voies aériennes supérieures laissent supposer une influence ethnique sur la survenue d'un SAOS. Il existe un risque 2 fois plus important de troubles respiratoires nocturnes chez les Américains d'origine africaine comparativement aux Américains d'origine caucasienne. Les sujets d'origine africaine présentent des troubles respiratoires nocturnes en moyenne 8,4 ans plus tôt que les patients d'origine caucasienne. Certaines pathologies endocrines, enfin, sont fréquemment associées à un SAOS, comme l'acromégalie, le syndrome de Cushing ou, surtout, une hypothyroïdie et un diabète. L'administration de certains médicaments comme les benzodiazépines (somnifères, anxiolytiques ..) et les bêtabloquants aggravent un SAOS. |
|
La mortalité des SAOS est
essentiellement
d'origine vasculaire. Au plan de la morbidité, les risques relatifs comparés à des sujets normaux de même âge sont de 2 fois plus d'hypertension artérielle (HTA), 3 fois plus d'insuffisance coronarienne et 4 fois plus d'accidents vasculaires cérébraux. L'influence du SAOS seul sur la mortalité reste cependant controversée et d'une grande actualité. Une première étude portant sur 20 sujets âgés ne constate aucune différence due à la présence d'événements respiratoires nocturnes dans les taux de morbidité et de mortalité. A l'opposé, d'autres auteurs trouvent, sur 385 sujets masculins suivis pendant 8 ans, une probabilité de survie cumulée nettement diminuée chez les patients ayant un IA > 20 (0,63) comparativement à celle (0,96) des patients avec un IA < 20 et ce, surtout pour les sujets âgés de moins de 50 ans. Une étude rapporte une mortalité triple chez les sujets âgés avec un IA > 10. Une étude récente portant sur 1620 patients avec SAOS montre un excès de mortalité pour les hommes de 40 à 60 ans et souligne le rôle délétère de l'obésité et de l'hypertension. Une étude rétrospective portant sur 3 100 hommes âgés de 30 à 69 ans a étudié la mortalité associée au ronflement et à la somnolence diurne excessive sur une période de 10 ans : une augmentation de mortalité (RR = 2,7) a été retrouvée chez les sujets de moins de 60 ans souffrant de ronchopathie et d'hypersomnolence diurne. |
SYMPTOMES RENCONTRÉS DANS UN SAOS
| ||||||||||||||||||||||
|
LES RONFLEMENTS
Le ronflement est un symptôme cardinal, existant chez 70 à 95% des patients présentant un SAOS. Il s'agit d'un bruit intense, entrecoupé de gargouillements, allant crescendo pour être interrompu par une apnée et réapparaître de façon explosive à la reprise ventilatoire. Souvent source de conflits conjugaux de part sa sonorité qui empêche le partenaire de chambre de dormir, il est provoqué par la mise en vibration des parties molles du pharynx comprenant la luette, le voile du palais et la base de la langue, mise en vibration secondaire aux turbulences du flux aérien inspiratoire. Il faut savoir qu'il existe des SAOS " silencieux " qui sont soit des SAOS extrêmement sévères s'accompagnant d'une insuffisance respiratoire ne permettant plus de générer les pressions et les débits suffisants pour produire le ronflement soit des SAOS continuant à se développer à bas bruit chez les patients ayant déjà bénéficié d'une uvulo-palato-pharyngoplastie.
Il reste que le ronflement est fréquent dans la population générale et n'est pas synonyme de SAOS. Les différentes études épidémiologiques montrent une prévalence dans la population générale de 19%. La prévalence augmente avec l'âge, dans les deux sexes après 35 ans, et l'on estime que 60% des hommes et 40% des femmes d'âge moyen (41 – 65 ans) sont des ronfleurs habituels. Les facteurs de risque du ronflement sont les mêmes que ceux du SAOS : facteurs anatomiques crânio-faciaux, sexe masculin, obésité et âge. Il est exacerbé par le décubitus dorsal, la prise de poids, la prise d'alcool, le tabagisme, la prise d'hypnotique et la privation de sommeil.
Il reste que le ronflement est fréquent dans la population générale et n'est pas synonyme de SAOS. Les différentes études épidémiologiques montrent une prévalence dans la population générale de 19%. La prévalence augmente avec l'âge, dans les deux sexes après 35 ans, et l'on estime que 60% des hommes et 40% des femmes d'âge moyen (41 – 65 ans) sont des ronfleurs habituels. Les facteurs de risque du ronflement sont les mêmes que ceux du SAOS : facteurs anatomiques crânio-faciaux, sexe masculin, obésité et âge. Il est exacerbé par le décubitus dorsal, la prise de poids, la prise d'alcool, le tabagisme, la prise d'hypnotique et la privation de sommeil.
LES APNÉES NOCTURNES
Rapportées par le conjoint pour lequel elles sont particulièrement angoissantes, ces pauses respiratoires sont de fréquence et de durée variable, pouvant dépasser les 30 secondes. Les patients peuvent rapporter, quant à eux, des sensations d'étouffement nocturne, les obligeant à s'asseoir voire à ouvrir la fenêtre. Elles sont décrites dans 65 à 92% des cas de SAOS authentifié par une polysomnographie (PSG) mais également retrouvées chez 31 à 64% des cas pour lesquels la PSG ne confirme pas le diagnostic.
AUTRES MANIFESTATIONS NOCTURNES
En plus des ronflements et des pauses respiratoires, d'autres manifestations nocturnes sont rencontrées :
Un sommeil agité et non réparateur – avec de nombreux mouvements accompagnant la survenue des apnées et la reprise ventilatoire
Des sueurs nocturnes, fréquentes (66% des cas), qui constituent un signe indirect avec l'existence d'un sommeil agité
Une nycturie retrouvée chez 28% des patients porteurs d'un SAOS. Ce symptôme serait lié à la sécrétion de facteur auriculaire natriurétique(FAN) provoquée par les variations importantes de pression intra-thoracique au cours des apnées. Plus rarement, on observe une énurésie chez 5% des patients.
On rapporte 10% de cas de somnambulisme dans une population de SAOS.
variable, pouvant dépasser les 30 secondes. Les patients peuvent rapporter, quant à eux, des sensations d'étouffement nocturne, les obligeant à s'asseoir voire à ouvrir la fenêtre. Elles sont décrites dans 65 à 92% des cas de SAOS authentifié par une polysomnographie (PSG) mais également retrouvées chez 31 à 64% des cas pour lesquels la PSG ne confirme pas le diagnostic.
AUTRES MANIFESTATIONS NOCTURNES
En plus des ronflements et des pauses respiratoires, d'autres manifestations nocturnes sont rencontrées :
Un sommeil agité et non réparateur – avec de nombreux mouvements accompagnant la survenue des apnées et la reprise ventilatoire
Des sueurs nocturnes, fréquentes (66% des cas), qui constituent un signe indirect avec l'existence d'un sommeil agité
Une nycturie retrouvée chez 28% des patients porteurs d'un SAOS. Ce symptôme serait lié à la sécrétion de facteur auriculaire natriurétique(FAN) provoquée par les variations importantes de pression intra-thoracique au cours des apnées. Plus rarement, on observe une énurésie chez 5% des patients.
On rapporte 10% de cas de somnambulisme dans une population de SAOS.
variable, pouvant dépasser les 30 secondes. Les patients peuvent rapporter, quant à eux, des sensations d'étouffement nocturne, les obligeant à s'asseoir voire à ouvrir la fenêtre. Elles sont décrites dans 65 à 92% des cas de SAOS authentifié par une polysomnographie (PSG) mais également retrouvées chez 31 à 64% des cas pour lesquels la PSG ne confirme pas le diagnostic.
L'HYPERSOMNOLENCE DIURNE
La déstructuration
du sommeil
liée à la fréquence des micro éveils et à la quasi absence de sommeil lent
profond provoque une hypersomnolence diurne, qui peut prendre des degrés très
divers. Elle va se manifester d'abord en période postprandiale puis survenir dès
que le patient n'est plus stimulé (lecture, tâches répétitives, conduite
monotone) pour devenir majeure, compromettant la vie familiale, sociale et
professionnelle du patien.
Évaluée par des échelles de somnolence comme la très classique échelle d'Epworth, elle peut être sous-estimée par le patient car elle fait partie de son quotidien depuis des mois voire des années. 40% des patients ayant un score à l'échelle d'Epworth inférieur à 12, et donc sans hypersomnolence diurne excessive, ont un IAH supérieur à 20. En outre, il ne faut pas négliger les patients qui n'ont aucun intérêt à se plaindre de leur somnolence comme les chauffeurs routiers ou les conducteurs de train et ce, de peur de perdre leur emploi.
La survenue d'endormissements chez les conducteurs automobiles est cependant une des conséquences les plus graves du SAOS en raison du risque d'accidents 2 à 3 fois supérieur à celui de la population générale, risque qui augmente avec la gravité du SAOS. Il est par ailleurs intéressant de noter qu'il n'existe pas de liens de proportionnalité entre la somnolence diurne évaluée par l'échelle d'Epworth ou objectivée au laboratoire par un test itératif de latence d'endormissement, d'une part, et les différents paramètres polysomnographiques témoignant de la sévérité du SAOS (IAH, micro éveils .. ), d'autre part.
Évaluée par des échelles de somnolence comme la très classique échelle d'Epworth, elle peut être sous-estimée par le patient car elle fait partie de son quotidien depuis des mois voire des années. 40% des patients ayant un score à l'échelle d'Epworth inférieur à 12, et donc sans hypersomnolence diurne excessive, ont un IAH supérieur à 20. En outre, il ne faut pas négliger les patients qui n'ont aucun intérêt à se plaindre de leur somnolence comme les chauffeurs routiers ou les conducteurs de train et ce, de peur de perdre leur emploi.
La survenue d'endormissements chez les conducteurs automobiles est cependant une des conséquences les plus graves du SAOS en raison du risque d'accidents 2 à 3 fois supérieur à celui de la population générale, risque qui augmente avec la gravité du SAOS. Il est par ailleurs intéressant de noter qu'il n'existe pas de liens de proportionnalité entre la somnolence diurne évaluée par l'échelle d'Epworth ou objectivée au laboratoire par un test itératif de latence d'endormissement, d'une part, et les différents paramètres polysomnographiques témoignant de la sévérité du SAOS (IAH, micro éveils .. ), d'autre part.
VALEUR PRÉDICTIVE DES SIGNES CLINIQUES
Nettement moins évocatrices,
ces manifestations sont cependant importantes à connaître et à rechercher. On
observe :
- Des céphalées matinales ou qui réveillent le patient. Elles peuvent persister plusieurs heures après le réveil et survenir après une sieste prolongée.
- Des troubles de la libido, en particulier chez l'homme – touchant jusqu'à 28% des patients
- La somnolence diurne peut interférer avec les fonctions intellectuelles. On ne sait si l'altération des fonctions supérieures (défaut de concentration et de l'attention, altération de la mémoire et du contrôle visuo-moteur) est liée à la somnolence ou à la pathologie respiratoire dans le sommeil et à l'hypoxémie.
- Des troubles de l'humeur et du comportement, avec irritabilité et même dépression, dont on ne sait également s'ils sont dus aux troubles du sommeil ou à la pathologie respiratoire dans le sommeil.
RETENTISSEMENTS DU SAOS
Rappelons que les
différentes études épidémiologiques réalisées chez les patients porteurs d'un
SAOS retrouvent une surmortalité liée à l'IAH, l'âge du patient, son poids ou
la présence d'une HTA concomitante. L'existence d'un SAOS augmente le risque
de voir survenir une hypertension artérielle systémique (HTA), des
troubles nocturnes du rythme cardiaque, un infarctus du myocarde, une
insuffisance cardiaque et une ischémie cérébrale.
- Le SAOS entraîne une importante fragmentation du sommeil.
En effet, chaque reprise ventilatoire au décours d'une apnée nécessite un allègement
du sommeil ou la survenue d'un micro éveil, causes d'une désorganisation
majeure du sommeil. L'index d'efficacité du sommeil est nettement diminué,
avec une augmentation de l'éveil intra-sommeil aux dépens de la durée
totale du sommeil. Le sommeil en lui-même s'approfondit peu, avec une
nette augmentation du sommeil lent léger (Stades I et II) aux dépens du
sommeil lent profond (Stades III et IV). Le sommeil paradoxal est quant à
lui également diminué.
- De nombreuses modifications cardio-vasculaires
aiguës, liées aux apnées et aux hypopnées, surviennent dans le
sommeil. Ces modifications hémodynamiques propres au SAOS viennent se
surajouter aux changements hémodynamiques spécifiques à chaque état de
vigilance.
RETENTISSEMENTS IMMÉDIATS
- Au cours du sommeil lent,
on observe une chute progressive physiologique de la fréquence cardiaque,
du débit cardiaque et de la pression artérielle. La chute du débit
cardiaque est liée à la réduction relative de la fréquence cardiaque, sans
modification du volume d'éjection systolique. La chute de la pression
artérielle est liée à la chute du débit cardiaque, sans modification des
résistances vasculaires périphériques. Ces modifications sont les plus
marquées au cours du stade IV de sommeil lent profond et sont
essentiellement liées à une augmentation du tonus vagal parasympathique au
cours du sommeil lent. Au cours du sommeil paradoxal, il existe, à
l'opposé, une grande variabilité du rythme cardiaque et de la pression
artérielle liée à une augmentation du tonus orthosympathique.
- Les patients atteints d'un
SAOS vont
présenter, au cours de la nuit, des oscillations permanentes de leurs
paramètres hémodynamiques (fréquence cardiaque, débit cardiaque,
pression artérielle). Ces oscillations sont liées tant à la survenue des
événements respiratoires nocturnes qu'aux changements rapides d'états de
vigilance (micro éveils) induits par ces anomalies ventilatoires. Elles
sont donc le résultat de l'intégration des réponses à 5 types de stimuli :
l'hypoxie, l'hypercapnie, les modifications de volume pulmonaire ou de
pression endothoracique, les micro éveils liés aux apnées comme le stade
de vigilance au cours duquel survient l'apnée. Si la bradycardie en cours
d'apnées continue à être décrite comme une manifestation classique du
SAOS, la tendance actuelle penche pour une accélération de la fréquence
cardiaque en cours d'apnée avec une augmentation supplémentaire lors
du micro éveil et de la reprise ventilatoire. Seuls 10% des patients,
porteurs de SAOS majeur et très désaturant, présenteraient des
bradycardies très sévères de fin d'apnée. La chute habituelle de la
pression artérielle observée au cours de la nuit chez le sujet normal
disparaît chez le patient apnéique et ce d'autant plus que le SAOS est
plus sévère. La pression artérielle atteint son niveau le plus bas au début
de l'apnée puis va crescendo pour atteindre son niveau maximum quelques
secondes après la reprise ventilatoire au moment du micro éveil – moment
où la SaO2 est minimale.
- La vitesse du flux sanguin
cérébral (VFSC) varie parallèlement à la pression artérielle. Pression
artérielle et VFSC augmentent donc au cours de l'apnée pour atteindre un
maximum au moment de la reprise ventilatoire. Il existe alors une chute
rapide de la pression artérielle et de la VFSC, qui devient inférieure aux
valeurs initiales. Avec la répétition des apnées, on peut donc observer
des périodes prolongées de diminution du débit sanguin cérébral. Cette diminution
du débit sanguin cérébral est liée à la longueur des événements
obstructifs et à la désaturation associée. La période d'hypotension
suivant immédiatement la reprise ventilatoire pendant laquelle l'hypoxémie
est importante et la perfusion cérébrale minimum correspond probablement
au moment où le cerveau est le plus vulnérable – tendant à expliquer le risque
accru d'accidents vasculaires cérébraux chez les patients apnéiques.
INSUFFISANCE RESPIRATOIRE CHRONIQUE
On sait depuis que l'on explore sur une grande
echelle les malades présentant un SAOS que la plupart d'entre eux n'ont pas
d'insuffisance respiratoire, définie par des troubles gazométriques diurnes ni
même par un déficit ventilatoire appréciable. Dans le cadre du SAOS, il
convient, en fait, de parler d'insuffisance respiratoire avec hypoxémie (PaO2
< 70 mm Hg) – hypercapnie (PaCO2 > 45 mm Hg) puisqu'une obésité isolée
importante peut induire une hypoxémie sans qu'il y ait d'insuffisance
respiratoire au sens strict; l'hypoxémie isolée peu importante est donc banale
chez les patients SAOS obèses. Sur 265 patients SAOS, la survenue d'une
hypoxémie, définie par une PaO2 < 65 mm Hg, n'est présente que dans 27% des
cas, la fréquence de l'hypercapnie n'étant que de 10%. L'hypoventilation
alvéolaire chronique étant la cause principale de l'hypertension artérielle
pulmonaire (HTAP) dans les affections respiratoires chroniques, il est
intéressant de constater que la prévalence de l'HTAP est également de 10% à 20%
des cas.
Les causes et les mécanismes de l'apparition d'une insuffisance respiratoire chronique (IRC) chez certains SAOS sont cependant loin d'être élucidées. Les facteurs incriminés sont :
- la sévérité du SAOS
- l'existence d'une éventuelle diminution de la
chémosensibilité chez certains de ces patients
- le rôle de l'obésité et, enfin,
- le rôle d'une broncho-pneumopathie chronique
obstructive (BPCO) associée.
Il n'a pas été possible de démontrer, jusque là, de relation entre la sévérité des événements respiratoires nocturnes et le niveau des gaz du sang artériels diurnes. Il n'est pas plus démontré actuellement qu'une hyposensibilité aux stimuli hypoxique et hypercapnique, peut-être induite par les effets à long terme de l'hypoventilation nocturne contemporaine des apnées, soit un facteur déterminant de l'IRC hypercapnique diurne.
L'obésité représente quant à elle un facteur non négligeable d'IRC dans le SAOS. L'hypoventilation alvéolaire survenant chez de grands obèses s'explique principalement par le coût excessif du travail respiratoire, du fait de la chute de la compliance du système respiratoire et de l'augmentation de la résistance thoracique. La corrélation entre l'élévation du coût en oxygène de la ventilation et le niveau de la PaCO2 est très significative chez les obèses. La fréquence de l'hypercapnie n'est pas plus grande chez les grands obèses (IMC > 40 kg/m2) avec SAOS que chez les autres.
Il ressort, en fait, de la plupart des travaux récents que l'obstruction chronique des voies aériennes distales est un facteur déterminant de l'IRC diurne dans le SAOS. L'association BPCO-SAOS est retrouvée dans 11% des cas. Dans les équations de régression multiple, le VEMS est le meilleur prédicteur de la PaO2 et de la PaCO2 chez les patients porteurs d'un SAOS; il est également un bon prédicteur du niveau de pression artérielle pulmonaire (PAP). Il reste que l'existence d'une BPCO est souvent méconnue et qu'elle peut être asymptomatique. Elle doit donc être systématiquement recherchée par des EFR. Elle représente sans doute le facteur déterminant de survenue d'une hypoventilation alvéolaire dans la plupart des cas de SAOS.
avec SAOS que chez les autres.
Il ressort, en fait, de la plupart des travaux
récents que l'obstruction chronique des voies aériennes distales est un facteur
déterminant de l'IRC diurne dans le SAOS. L'association
BPCO-SAOS est retrouvée dans 11% des cas. Dans les équations de
régression multiple, le VEMS est le meilleur prédicteur de la PaO2 et de la
PaCO2 chez les patients porteurs d'un SAOS; il est également un bon prédicteur
du niveau de pression artérielle pulmonaire (PAP). Il reste que l'existence
d'une BPCO est souvent méconnue et qu'elle peut être asymptomatique. Elle doit
donc être systématiquement recherchée par des EFR. Elle représente sans doute
le facteur déterminant de survenue d'une hypoventilation alvéolaire dans la
plupart des cas de SAOS.
EFFETS CARDIOVASCULAIRES CHRONIQUES
I

l n'y a actuellement pas de preuve que le SAOS, en l'absence d'hypoxémie ou d'hypoxémie-hypercapnie diurne, soit capable d'induire une HTAP permanente. L'HTAP est une conséquence de l'hypoxie alvéolaire prolongée tant nocturne, prononcée, que diurne, modérée. En outre, cette HTAP est le plus souvent modérée. Cette HTAP modérée n'exclut cependant pas le développement d'une insuffisance cardiaque droite à la faveur d'une surinfection broncho-pulmonaire aiguë.
Le système nerveux
autonome (SNA)
joue un rôle essentiel dans les mécanismes physiopathologiques à l'origine des
conséquences cardio-vasculaires aiguës et
chroniques du SAOS. Il apparaît, en fait, une élévation chronique du tonus
adrénergique
chez ces patients. La stimulation hypoxique répétée et l'obésité sont elles
mêmes associées à une augmentation de l'activité sympathique et pourraient
constituer des facteurs confondants essentiels. Mais, on a pu montrer que le
tonus adrénergique est augmentée de façon significative chez les patients obèses
ayant un SAOS modéré (IAH moyen = 19) et très peu de désaturations nocturnes
(SaO2 moyenne = 97%) ; en outre, l'obésité sans apnées n'est pas associée à une
augmentation du tonus adrénergique à destinée musculaire. Les mécanismes de
cette activation sympathique sont donc loin d'être élucidés. En outre, les
sujets apnéiques développent une sensibilité cardio-vasculaire excessive à la
stimulation sympathique de part la modification de la réponse endothéliale,
avec un déficit de la vasodilatation NO-dépendante. Le SAOS est également
associé à une réduction du tonus parasympathique. Les mécanismes à l'origine de ces
réponses vagales anormales ne sont pas élucidés.
Des études chez l'animal ont pu montrer que la répétition d'événements apnéiques sur plusieurs semaines était capables d'induire une HTA permanente, la survenue de celle-ci nécessitant une hypoxémie associée aux apnées – avec un système sympathique et des chémorécepteurs carotidiens intacts. La reprise ventilatoire postapnéique entraîne une hyperventilation, qui, si les réponses chémosensibles sont préservées, induit une hyperoxie transitoire et relative. Cette dernière génère un effet vasoconstricteur systémique qui va, en se répétant à chaque hypoxie intermittente, contribuer à modifier la structure endothéliale et augmenter de façon permanente les résistance vasculaires périphériques. En effet, la désactivation du chémoréflexe par inhalation de 100% d'oxygène durant 15 minutes entraîne une baisse significative du tonus sympathique musculaire et de la pression artérielle moyenne chez les patients apnéiques.
Des études chez l'animal ont pu montrer que la répétition d'événements apnéiques sur plusieurs semaines était capables d'induire une HTA permanente, la survenue de celle-ci nécessitant une hypoxémie associée aux apnées – avec un système sympathique et des chémorécepteurs carotidiens intacts. La reprise ventilatoire postapnéique entraîne une hyperventilation, qui, si les réponses chémosensibles sont préservées, induit une hyperoxie transitoire et relative. Cette dernière génère un effet vasoconstricteur systémique qui va, en se répétant à chaque hypoxie intermittente, contribuer à modifier la structure endothéliale et augmenter de façon permanente les résistance vasculaires périphériques. En effet, la désactivation du chémoréflexe par inhalation de 100% d'oxygène durant 15 minutes entraîne une baisse significative du tonus sympathique musculaire et de la pression artérielle moyenne chez les patients apnéiques.
TRAITEMENT DU SYNDROME D'APNÉES DU SOMMEIL
En France, les caisses d'assurance maladie
prennent en charge les patients atteints d'un SAS sévère se plaignant
d'hypersomnolence et d'au moins trois des signes suivants : ronflements,
nycturie, céphalées matinales, troubles de la libido, hypertension artérielle.
Ces signes doivent s'accompagner soit d'un IAH > 30 soit d'un IAH > 20
avec la survenue d'au moins 10 micro-éveils par heure de sommeil -
micro-éveils liés aux événements respiratoires nocturnes.
TRAITEMENTS MÉDICAUX
Considérée actuellement comme la méthode de référence, la
pression positive continue (PPC) a l'avantage de ne pas modifier
l'anatomie et donc, d'être peu agressive à l'opposé de l'ancien traitement de
référence qui était la trachéotomie. La pression positive correspond à une
pression supérieure à la pression atmosphérique appliquée de façon continue par
voie nasale ou nasofaciale, qui empêche l'occlusion des VAS et donc,
l'apparition des apnées dans le sommeil. Elle ne présente aucune
contre-indication et pas d'effets secondaires majeurs hormis :
- Une possible irritation locale liée au port du masque
- Des phénomènes d'hypersécrétion nasale avec rhinite
- Des phénomènes de conjonctivite liés à des fuites au masque
- Un assèchement de la muqueuse oropharyngée.
TRAITEMENTS CHIRURGICAUX
Le traitement chirurgical vise à une levée
radicale de l'obstacle oropharyngé. Il s'adresse tant au SAOS avec site
obstructif spécifique qu'au SAOS sans site obstructif évident. Dans ce dernier
cas, il tente soit :
Les résultats inconstants de ces techniques chirurgicales sont liés :
- de diminuer le volume des tissus mous (voile du palais, amygdales, base de la langue) limitant les parois de l'oropharynx
- de transférer vers l'avant les insertions de la langue et/ou les insertions du voile.
Les résultats inconstants de ces techniques chirurgicales sont liés :
- aux difficultés de l'évaluation préopératoire du site obstructif
- au caractère multifactoriel du SAOS.
LA PRESSION POSITIVE CONTINUE
L'envoi d'air à une pression suffisante pour maintenir les voies aériennes supérieures ouvertes malgrè la diminution du tonus musculaire des muscles dilatateurs du pharynx dans le sommeil permet la disparition des apnées. L'instauration du traitement nécessite une PSG de titration, permettant de régler le niveau de pression nécessaire à la disparition des apnées et de la ronchopathie comme à la restauration de l'organisation générale du sommeil. Le niveau de pression efficace doit être déterminé dans tous les stades de sommeil et dans toutes les positions du corps, en particulier le décubitus dorsal; il doit être systématiquement vérifié en sommeil paradoxal, et plus particulièrement en fin de nuit où le risque de récidive des troubles respiratoires est important; il est généralement établi entre 8 et 12 cm d'H2O avec des valeurs extrêmes de 5 à 18 cm d'H2O.
Dès la première nuit de traitement sous PPC, on observe une augmentation importante de la proportion en sommeil lent profond et en sommeil paradoxal, avec souvent un phénomène de rebond; le réveil s'accompagne d'une sensation de repos inhabituelle, de sommeil récupérateur avec une régression de l'hypersomnolence diurne, bon facteur de pronostic quant à l'observance future du traitement. Le rebond en sommeil lent profond et en sommeil paradoxal peut se poursuivre pendant toute la première semaine de traitement avant d'observer une normalisation complète de l'architecture du sommeil. Cependant, une étude récente comparant PPC contre placebo (PPC à une pression inefficace) montre des résultats très inattendus avec, au bout de 7 jours de traitement, une réelle efficacité de la PPC sur les événements respiratoires nocturnes, sur les micro éveils et sur la saturation nocturne sans amélioration de la qualité du sommeil. La plupart des études mettent néanmoins en évidence une amélioration significative de la latence d'endormissement au test itératif de latence d'endormissement ou au test de maintien de l'éveil sous PPC et ce, par rapport à l'état initial. Des résultats préliminaires pourraient faire évoquer une amélioration des chiffres tensionnels et ce indépendamment d'un amaigrissement concomitant mais associée à une correction de la saturation en oxygène et à une diminution de la sécrétion de catécholamines, l'effet du traitement par PPC sur l'hypertension artérielle restant à confirmer.
Quoiqu'il en soit, l'utilisation de la PPC s'accompagne d'une réduction de la mortalité comparable à celle obtenue après trachéotomie et supérieure au traitement chirurgical conventionnel ou après perte de poids isolée. En outre, elle améliore significativement, après 9 mois de traitement, les tests de performance lors d'une simulation de conduite automobile et ce, sans différence par rapport à un groupe témoin de sujets sains et réduit les accidents de circulation. L'amélioration de la qualité de vie et la disparition de l'angoisse des conjoints vis-à-vis des apnées nocturnes jouent un rôle dans la tolérance et l'observance du traitement.
Toute la limitation du traitement repose, en fait, sur la contrainte journalière qu'il impose aux malades. Après la première PSG de titration, le taux d'acceptation de la PPC varie entre 70 et 80%. A distance, 80 à 90% des patients continuent d'utiliser leur appareil à domicile avec, cependant, des durées d'utilisation très variables.
La qualité de l'observance est liée principalement à la qualité de la prise en charge des patients lors des premiers jours du traitement et avant leur retour à domicile. Elle dépend également de la gravité du SAOS et du degré d'hypersomnolence diurne initiaux.
TRAITEMENT CHIRURGICAL DU SAOS SANS SITE OBSTRUCTIF
La difficulté majeure est de
sélectionner les patients ayant un site obstructif unique, vélo-amygdalien ou
rétro-lingual, des patients ayant une atteinte bifocale.
La chirurgie hyoïdienne consiste à antérioriser l'os hyoïde. La transposition génienne vise à antérioriser les insertions de la langue. Les avancées maxillo-mandibulaires tentent d'antérioriser dans le même temps opératoire la mandibule et le maxillaire supérieur. La chirurgie maxillo-mandibulaire est une chirurgie efficace avec un taux de succès variant entre 65 et 100% pour un IAH postopératoire inférieur à 10.
La chirurgie du SAOS a été largement dominée par l'UPP. L'échec de cette chirurgie, en particulier pour les SAOS moyens ou sévères, comme le pourcentage non négligeable de patients abandonnant le traitement par PPC ont conduit les équipes chirurgicales à proposer divers traitements de l'oropharynx inférieur rétro-basilingual. Si les taux de succès des chirurgies du SAOS sont bien inférieurs à ceux de la PPC, il ne faut pas oublier qu'elles s'adressent à des patients le plus souvent en impasse thérapeutique pour lesquels il n'y a pas d'autre solution hormis les orthèses. Restent :
Le traitement postural visant à empêcher le patient de dormir en décubitus dorsal, efficace dans certains cas de SAOS peu sévères et dépendant de la position nocturne du patient
La chirurgie nasale indiquée quand elle permet une meilleure tolérance à la PPC ou en association avec les autres chirurgies du SAOS. Elle vise à la reperméation des fosses nasales par redressement du septum, résection de cornets nasaux hypertrophiques ou ablation de polypes nasaux.
Bien que rare, l'existence d'un site obstructif spécifique doit être recherché d'emblée chez un patient suspect de SAOS, nécessitant un examen ORL systématique. Les pathologies tumorales, bénignes ou malignes, de la base de la langue, de l'épiglotte ou des amygdales, les pathologies malformatives telles que les micrognathies, les séquelles traumatiques en particulier au niveau de l'articulation temporo-mandibulaire, une hypertrophie de la base de la langue dans le cadre d'une acromégalie, les pathologies laryngées obstructives sont autant de cas spécifiques nécessitant une prise en charge adaptée.
TRAITEMENTS CHIRURGICAUX DES TISSUS MOUS DE L'OROPHARYNX
- L'uvulo-palato-pharyngoplastie (UPP) ou pharyngotomie. Elle consiste en une excision de la luette, du voile du palais, des amygdales, et, éventuellement, d'une partie de la muqueuse de la paroi postérieure du pharynx, le but étant de restaurer une perméabilité normale des VAS. Les suites opératoires sont marquées par un syndrome algique important, des risques hémorragiques per- et postopératoires, des reflux liquidiens, une voix nasonnée, une dysphagie, des infections et la possibilité, à plus long terme, d'une sténose ou d'une insuffisance vélaire liée à un défaut de technique. Le taux d'efficacité subjective sur le ronflement est, en moyenne, supérieur à 80%. Si l'on considère un IAH inférieur à 10 comme critère de succès, le taux d'efficacité sur la régression des apnées est compris entre 40 et 50%. Une grande obésité (IMC > 30 kg/m2), un IAH élevé (> 30) et un âge avancé sont des facteurs prédictifs d'un échec de l'UPP.
- La pharyngotomie par laser ambulatoire. Apparue au début des années 90, cette technique a connu un développement important de part son faible coût et sa réalisation en ambulatoire. Elle ne peut pas être proposée en cas d'hypertrophie des amygdales et ne permet pas une plastie d'élargissement de l'oropharynx. Principalement indiquée dans le traitement des ronchopathies, elle donne un taux d'efficacité sur le ronflement à peu près identique à celui obtenu par la pharyngotomie classique.
- Les chirurgies linguales ont été développées en réponse à l'échec des chirurgies du voile du palais dans le cas des obstructions des VAS situées en arrière de la base de la langue.
CHIRURGIES OSSEUSES HYOÏDIENNES OU MAXILLO-MANDIBULAIRES
La chirurgie hyoïdienne consiste à antérioriser l'os hyoïde. La transposition génienne vise à antérioriser les insertions de la langue. Les avancées maxillo-mandibulaires tentent d'antérioriser dans le même temps opératoire la mandibule et le maxillaire supérieur. La chirurgie maxillo-mandibulaire est une chirurgie efficace avec un taux de succès variant entre 65 et 100% pour un IAH postopératoire inférieur à 10.
La chirurgie du SAOS a été largement dominée par l'UPP. L'échec de cette chirurgie, en particulier pour les SAOS moyens ou sévères, comme le pourcentage non négligeable de patients abandonnant le traitement par PPC ont conduit les équipes chirurgicales à proposer divers traitements de l'oropharynx inférieur rétro-basilingual. Si les taux de succès des chirurgies du SAOS sont bien inférieurs à ceux de la PPC, il ne faut pas oublier qu'elles s'adressent à des patients le plus souvent en impasse thérapeutique pour lesquels il n'y a pas d'autre solution hormis les orthèses. Restent :
Le traitement postural visant à empêcher le patient de dormir en décubitus dorsal, efficace dans certains cas de SAOS peu sévères et dépendant de la position nocturne du patient
La chirurgie nasale indiquée quand elle permet une meilleure tolérance à la PPC ou en association avec les autres chirurgies du SAOS. Elle vise à la reperméation des fosses nasales par redressement du septum, résection de cornets nasaux hypertrophiques ou ablation de polypes nasaux.
Bien que rare, l'existence d'un site obstructif spécifique doit être recherché d'emblée chez un patient suspect de SAOS, nécessitant un examen ORL systématique. Les pathologies tumorales, bénignes ou malignes, de la base de la langue, de l'épiglotte ou des amygdales, les pathologies malformatives telles que les micrognathies, les séquelles traumatiques en particulier au niveau de l'articulation temporo-mandibulaire, une hypertrophie de la base de la langue dans le cadre d'une acromégalie, les pathologies laryngées obstructives sont autant de cas spécifiques nécessitant une prise en charge adaptée.
LES RÈGLES HYGIÉNO-DIÉTÉTIQUES
L'objectif principal est la
perte de poids. Ces mesures n'ont fréquemment qu'une efficacité incomplète et
temporaire. Les règles hygiéno-diététiques visent à supprimer ou à limiter les
facteurs qui favorisent l'obstruction pharyngée, tels que le surpoids, la prise
de boissons alcoolisées, le tabac, les somnifères et le sommeil en décubitus
dorsal. La perte de poids peut entraîner une amélioration clinique mais son
efficacité sur l'élimination des apnées est moins certaine et concerne surtout
les obésités morbides.
LES ORTHÈSES ENDOBUCCALES
Les orthèses endobuccales
représentent une alternative aux traitements habituellement proposés et à la PPC
en particulier. En effet, en France, la PPC est réservée aux patients dont l'IAH
est supérieur ou égal à 30 ou, maintenant, à ceux dont l'index est inférieur à
30 avec un index de micro éveils nocturnes liés aux apnées-hypopnées supérieur à
10 par heure. Doivent s'associer à cet IAH un cortège de symptômes témoignant
d'une déstructuration du sommeil. En outre, une mauvaise acceptation
psychologique de la PPC peut aboutir, chez certains patients, à un arrêt du
traitement ou, pour tout le moins, à une mauvaise compliance responsable de la
persistance de la symptomatologie initiale tant diurne que nocturne. Les
résultats actuels orientent plutôt vers la possibilité de la prise en charge par
orthèse endobuccale des formes peu sévères ou modérées de SAOS. Le but de ces
orthèses est d'agrandir et/ou de stabiliser les VAS pendant le sommeil. Seuls
l'avancement mandibulaire et la protrusion de la langue ont montré une
efficacité clinique.
Les orthèses d'avancement mandibulaire avancent la mandibule de 5 mm environ pour agrandir la filière aérienne pharyngée postérieure, écartant les structures anatomiques collabables entre elles. On solidarise, par une orthèse monobloc ou bibloc, la mandibule physiologiquement mobile au maxillaire fixe par des gouttières fixées aux arcades dentaires et solidarisées entre elles. Une revue de la littérature fait état de 73 à 100% de réussite chez les ronfleurs. Il reste que peu d'études rapportent une analyse objective de cette amélioration, qui est inversement proportionnelle à la gravité du SAOS concomitant à la ronchopathie. Sur le plan des apnées, 70% des patients voient leur IAH diminuer de 50%, 51% d'entre eux avec un IAH inférieur à 10. Il existe ici aussi une relation inversement proportionnelle entre le niveau de gravité initiale et la diminution de l'IAH. De fait, des études récentes ont comparé les effets et la tolérance des orthèse d'avancement mandibulaire au traitement par PPC ; dans le cas des SAOS peu sévères à modérés, les conclusions sont à l'avantage des orthèses, la PPC conservant toute sa place dans les formes sévères. Les effets secondaires sont :
La compliance au traitement dépend essentiellement de l'existence ou non d'effets secondaires, le maintien de l'utilisation de la pièce étant inversement proportionnel à la durée du suivi.
Les orthèses de protrusion de la langue avancent la masse linguale en libérant l'espace pharyngé postérieur soit en tirant soit en poussant sur la langue. Les différentes études rapportent une diminution de l'IAH d'environ 50% et ceux chez les patients particulièrement compliants. Globalement, ces dispositifs sont mal tolérés avec algies de la langue et hypersialorrhée diminuant la tolérance.
Les orthèses d'avancement mandibulaire avancent la mandibule de 5 mm environ pour agrandir la filière aérienne pharyngée postérieure, écartant les structures anatomiques collabables entre elles. On solidarise, par une orthèse monobloc ou bibloc, la mandibule physiologiquement mobile au maxillaire fixe par des gouttières fixées aux arcades dentaires et solidarisées entre elles. Une revue de la littérature fait état de 73 à 100% de réussite chez les ronfleurs. Il reste que peu d'études rapportent une analyse objective de cette amélioration, qui est inversement proportionnelle à la gravité du SAOS concomitant à la ronchopathie. Sur le plan des apnées, 70% des patients voient leur IAH diminuer de 50%, 51% d'entre eux avec un IAH inférieur à 10. Il existe ici aussi une relation inversement proportionnelle entre le niveau de gravité initiale et la diminution de l'IAH. De fait, des études récentes ont comparé les effets et la tolérance des orthèse d'avancement mandibulaire au traitement par PPC ; dans le cas des SAOS peu sévères à modérés, les conclusions sont à l'avantage des orthèses, la PPC conservant toute sa place dans les formes sévères. Les effets secondaires sont :
- Une hypersialorrhée
- Un inconfort dentaire après l'éveil
- Une sécheresse de la bouche
- Et surtout, des douleurs au niveau des articulations temporo-mandibulaires.
La compliance au traitement dépend essentiellement de l'existence ou non d'effets secondaires, le maintien de l'utilisation de la pièce étant inversement proportionnel à la durée du suivi.
Les orthèses de protrusion de la langue avancent la masse linguale en libérant l'espace pharyngé postérieur soit en tirant soit en poussant sur la langue. Les différentes études rapportent une diminution de l'IAH d'environ 50% et ceux chez les patients particulièrement compliants. Globalement, ces dispositifs sont mal tolérés avec algies de la langue et hypersialorrhée diminuant la tolérance.
Inscription à :
Articles (Atom)